Оглавление
- 1 Связанные заболевания и их лечение
- 2 Классификация острого инфаркта миокарда
- 3 Содержание инструкции
- 4 Названия
- 5 Описание
- 6 Дополнительные факты
- 7 Причины
- 8 Классификация
- 9 Симптомы
- 10 Возможные осложнения
- 11 Диагностика
- 12 Лечение
- 13 Прогноз
- 14 Профилактика
- 15 Названия
- 16 Латинское название
- 17 Химическое название
- 18 Фарм Группа
- 19 Нозологии
- 20 Код CAS
- 21 Характеристика вещества
- 22 Фармакодинамика
- 23 Показания к применению
- 24 Противопоказания
- 25 Ограничения к использованию
- 26 Применение при беременности и кормлении грудью
- 27 Побочные эффекты
- 28 Взаимодействие
- 29 Передозировка
- 30 Способ применения и дозы
- 31 Меры предосторожности применения
- 32 Первая помощь при инфаркте
- 33 Описание
- 34 Дополнительные факты
- 35 Диагностика
- 36 Прогноз
Связанные заболевания и их лечение
При инфаркте миокарда показана экстренная госпитализация в кардиологическую реанимацию. В остром периоде пациенту предписывается постельный режим и психический покой, дробное, ограниченное по объему и калорийности питание. В подостром периоде больной переводится из реанимации в отделение кардиологии, где продолжается лечение инфаркта миокарда и осуществляется постепенное расширение режима.
Купирование болевого синдрома проводится сочетанием наркотических анальгетиков (фентанила) с нейролептиками (дроперидолом), внутривенным введением нитроглицерина. Терапия при инфаркте миокарда направлена на предупреждение и устранение аритмий, сердечной недостаточности, кардиогенного шока. Назначают антиаритмические средства (лидокаин), ß-адреноблокаторы (атенолол), тромболитики (гепарин, ацетилсалициловая к-та), антогонисты Са (верапамил), магнезию, нитраты, спазмолитики.
Классификация острого инфаркта миокарда
Патологию классифицируют по времени возникновения, локализации, распространенности и глубине поражения, а также по характеру протекания.
По времени возникновения выделяют:
- острый инфаркт – возникший впервые;
- повторный инфаркт – возникший в течение 8 недель после первого;
- рецидивирующий – развивается по истечению 8 недель после первичного.
Очаг повреждения тканей чаще всего локализируется в области верхушки сердца, передней и боковой стенок левого желудочка и в передних отделах межжелудочковой перегородки, то есть в бассейне передней межжелудочковой ветви левой коронарной артерии. Реже инфаркт возникает в области задней стенки левого желудочка и задних отделов межжелудочковой перегородки, то есть в бассейне огибающей ветви левой коронарной артерии.
В зависимости от глубины поражения инфаркт бывает:
- субэндокардиальный – узкий некротический очаг проходит вдоль эндокарда левого желудочка;
- субэпикардиальный – очаг некроза локализуется возле эпикарда;
- интрамуральный – находится в толще сердечной мышцы, не касаясь верхнего и нижнего слоев;
- трансмуральный – поражает всю толщину стенки сердца.
В протекании заболевания выделяют четыре стадии – острейшая, острая, подострая, стадия рубцевания. Если рассматривать патологический процесс с точки зрения патанатомии, можно выделить два основных периода:
- Некротический. Образуется зона некроза тканей, зона асептического воспаления вокруг нее с присутствием большого количества лейкоцитов. От дисциркуляторных нарушений страдают окружающие ткани, причем нарушения могут наблюдаться далеко за пределами сердца, даже в головном мозге.
- Организация (рубцевание). В очаг прибывают макрофаги и фибробласты – клетки, которые способствуют росту соединительной ткани. Макрофаги поглощают некротические массы, а клетки фибробластического ряда наполняют образовавшуюся полость соединительной тканью. Этот период длится до 8 недель.
Большой процент смертности от инфаркта приходится не на первичное заболевание, а на его осложнения. Развитие осложнений зависит от объема помощи, оказанной в острейший период и в стадии рубцевания. Часты случаи, когда больные, успешно пережившие инфаркт, через несколько месяцев умирали из-за отсроченных осложнений – вот почему крайне важно отнестись ответственно к врачебным рекомендациям и продолжать поддерживающее лечение.
Осложнения инфаркта делят на ранние, возникающие в первые 8 недель после манифестации, и поздние, развивающиеся спустя 8 недель.
К ранним относятся:
- кардиогенный шок – состояние, характеризующееся несоответствием между выбросом сердцем порции крови и периферическим сопротивлением сосудов. Возникает острая сердечная недостаточность, при этом от стресса сосуды спазмируются, что еще больше усугубляет положение;
- миомаляция – расплавление некротизированного миокарда, когда доминирует автолиз поврежденных тканей. Этот процесс практически необратим, ведет к истончению стенки сердца, разрыву сердца, кровоизлияниям в перикард (следствием является тампонада сердца);
- острая аневризма сердца – возможна при массивных инфарктах, когда некротизированная стенка выбухает наружу, образуя пространство, быстро заполняющееся кровью, которая плохо оттекает. Часто в таких полостях формируются тромбы, эндокард со временем надрывается, а вскоре патологический процесс распространяется и на другие участки сердца;
- пристеночные тромбы – образуются в отсутствие адекватного лечения фибринолитиками. Опасность в повышении риска периферических тромбоэмболических осложнений;
- перикардит – воспаление оболочек сердца, частое раннее осложнение инфаркта миокарда трансмурального типа. Асептическое воспаление усугубляется присоединением аутоиммунных процессов;
- фибрилляция желудочков – одно из самых опасных расстройств проводимости и возбудимости сердечной ткани, при котором сердце не может совершить толчок и просто дрожит, а циркуляция крови в организме практически останавливается;
- реперфузионный синдром – за время отсутствия кровотока в пораженных тканях накапливается множество метаболитов, застрявших на промежуточных звеньях переработки. Если инфаркт длится больше 40 минут, а после этого были резко введены фибринолитики, кровь немедленно поступает в пораженную область и активирует все накопившиеся реакции. В результате выделяется множество окислителей, которые еще больше повреждают очаг инфаркта.
Поздние осложнения:
- хроническая сердечная недостаточность – состояние, при котором поврежденное сердце из-за соединительнотканного рубца не в состоянии в полной мере обеспечить организм необходимыми объемами крови, страдает его насосная функция;
- синдром Дресслера – аутоимунное заболевание, при котором к некротизированной ткани вырабатываются антитела, которые еще больше усиливают воспаление и разрушение в зоне инфаркта;
- кардиосклероз – замещение специфичных тканей сердца соединительной тканью, которая обладает низкой способностью к эластичному растяжению, не может активно сокращаться. В результате при увеличении давления или объема крови в сердце стенка может истончаться и раздуваться.
Отсроченные осложнения незначительно ухудшают уровень жизни больного, но обладают высоким риском летальности.
 После перенесенного инфаркта обо всех изменениях в самочувствии необходимо извещать врача
После перенесенного инфаркта обо всех изменениях в самочувствии необходимо извещать врачаБольной должен быть осведомлен о возможных осложнениях в ходе рекреации, чтобы вовремя предупредить родных и лечащего врача о любых изменениях в своем состоянии. Инфаркт и его осложнения обязательно вносятся в историю болезни, на случай если с больным будет работать другой врач. Клинические рекомендации обязательно включают профилактику рецидива инфаркта и поздних осложнений.
В соответствии с размерами очагового поражения сердечной мышцы выделяют инфаркт миокарда: • крупноочаговый. • мелкоочаговый. На долю мелкоочаговых инфарктов миокарда приходится около 20% клинических случаев, однако нередко мелкие очаги некроза в сердечной мышце могут трансформироваться в крупноочаговый инфаркт миокарда (у 30% пациентов).

В отличие от крупноочаговых, при мелкоочаговых инфарктах не возникают аневризма и разрыв сердца, течение последних реже осложняется сердечной недостаточностью, фибрилляцией желудочков, тромбоэмболией. В зависимости от глубины некротического поражения сердечной мышцы выделяют инфаркт миокарда: • трансмуральный – с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый).
• интрамуральный – с некрозом в толще миокарда. • субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду. • субэпикардиальный – с некрозом миокарда в зоне прилегания к эпикарду. По изменениям, фиксируемым на ЭКГ, различают. • «Q-инфаркт» – с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще крупноочаговый трансмуральный инфаркт миокарда).
• «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще мелкоочаговый инфаркт миокарда). По топографии и в зависимости от поражения определенных ветвей коронарных артерий инфаркт миокарда делится на: • правожелудочковый. • левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки.
По кратности возникновения различают инфаркт миокарда: • первичный. • рецидивирующий (развивается в срок 8 недель после первичного). • повторный (развивается спустя 8 недель после предыдущего). По развитию осложнений инфаркт миокарда подразделяется на: • осложненный. • неосложненный По наличию и локализации болевого синдрома.
коллаптоидная, астматическая, отечная, аритмическая, церебральная. • малосимптомную (стертую). • комбинированную. В соответствии с периодом и динамикой развития инфаркта миокарда выделяют: • стадию ишемии (острейший период). • стадию некроза (острый период). • стадию организации (подострый период). • стадию рубцевания (постинфарктный период).
Нередко осложнения возникают уже в первые часы и дни инфаркта миокарда, утяжеляя его течение. У большинства пациентов в первые трое суток наблюдаются различные виды аритмий: экстрасистолия, синусовая или пароксизмальная тахикардия, мерцательная аритмия, полная внутрижелудочковая блокада. Наиболее опасно мерцание желудочков, которое может перейти в фибрилляцию и привести к гибели пациента.
Левожелудочковая сердечная недостаточность характеризуется застойными хрипами, явлениями сердечной астмы, отека легких и нередко развивается в острейший период инфаркта миокарда. Крайне тяжелой степенью левожелудочковой недостаточности является кардиогенный шок, развивающийся при обширном инфаркте и обычно приводящий к летальному исходу.
Признаками кардиогенного шока служит падение систолического АД ниже 80 мм , нарушение сознания, тахикардия, цианоз, уменьшение диуреза. Разрыв мышечных волокон в зоне некроза может вызывать тампонаду сердца – кровоизлияние в полость перикарда. У 2-3% пациентов инфаркт миокарда осложняется тромбоэмболиями системы легочной артерии (могут стать причиной инфаркта легких или внезапной смерти) или большого круга кровообращения.
Пациенты с обширным трансмуральным инфарктом миокарда в первые 10 суток могут погибнуть от разрыва желудочка вследствие острого прекращения кровообращения. При обширном инфаркте миокарда может возникать несостоятельность рубцовой ткани, ее выбухание с развитием острой аневризмы сердца. Острая аневризма может трансформироваться в хроническую, приводящую к сердечной недостаточности.
Отложение фибрина на стенках эндокарда приводит к развитию пристеночного тромбоэндокардита, опасного возможностью эмболии сосудов легких, мозга, почек оторвавшимися тромботическими массами. В более позднем периоде может развиться постинфарктный синдром, проявляющийся перикардитом, плевритом, артралгиями, эозинофилией.
Содержание инструкции
Названия
Название: Инфаркт миокарда.
Описание
Инфаркт миокарда. Очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
Дополнительные факты
Инфаркт миокарда. Очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
В возрасте 40-60 лет инфаркт миокарда в 3–5 раз чаще наблюдается у мужчин в связи с более ранним (на 10 лет раньше, чем у женщин) развитием атеросклероза. После 55-60 лет заболеваемость среди лиц обоего пола приблизительно одинакова. Показатель летальности при инфаркте миокарда составляет 30—35%. Статистически 15—20% внезапных смертей обусловлены инфарктом миокарда.
Нарушение кровоснабжения миокарда на 15-20 и более минут приводит к развитию необратимых изменений в сердечной мышце и расстройству сердечной деятельности. Острая ишемия вызывает гибель части функциональных мышечных клеток (некроз) и последующее их замещение волокнами соединительной ткани, т. Е. Формирование постинфарктного рубца.
В клиническом течении инфаркта миокарда выделяют пять периодов:
• 1 период. Предынфарктный (продромальный) – учащение и усиление приступов стенокардии, может продолжаться несколько часов, суток, недель;
• 2 период. Острейший – от развития ишемии до появления некроза миокарда, продолжается от 20 минут до 2 часов;
• 3 период. Острый – от образования некроза до миомаляции (ферментативного расплавления некротизированной мышечной ткани), длительность от 2 до 14 суток;
• 4 период. Подострый – начальные процессы организации рубца, развитие грануляционной ткани на месте некротической, продолжительность 4 – 8 недель;
• 5 период. Постинфарктный – созревание рубца, адаптация миокарда к новым условиям функционирования.
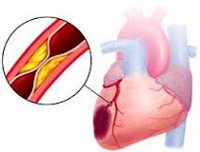
Причины
Инфаркт миокарда является острой формой ИБС. В 97—98% случаев основой для развития инфаркта миокарда служит атеросклеротическое поражение венечных артерий, вызывающее сужение их просвета. Нередко к атеросклерозу артерий присоединяется острый тромбоз пораженного участка сосуда, вызывающий полное или частичное прекращение кровоснабжения соответствующей области сердечной мышцы. Тромбообразованию способствует повышенная вязкость крови, наблюдаемая у пациентов с ИБС. В ряде случаев инфаркт миокарда возникает на фоне спазма ветвей венечных артерий.
Развитию инфаркта миокарда способствуют сахарный диабет, гипертоничесая болезнь, ожирение, нервно-психическое напряжение, увлечение алкоголем, курение. Резкое физическое или эмоциональное напряжение на фоне ИБС и стенокардии может спровоцировать развитие инфаркта миокарда. Чаще развивается инфаркт миокарда левого желудочка.
Классификация
В соответствии с размерами очагового поражения сердечной мышцы выделяют инфаркт миокарда:
• крупноочаговый.
• мелкоочаговый.
На долю мелкоочаговых инфарктов миокарда приходится около 20% клинических случаев, однако нередко мелкие очаги некроза в сердечной мышце могут трансформироваться в крупноочаговый инфаркт миокарда (у 30% пациентов). В отличие от крупноочаговых, при мелкоочаговых инфарктах не возникают аневризма и разрыв сердца, течение последних реже осложняется сердечной недостаточностью, фибрилляцией желудочков, тромбоэмболией.
В зависимости от глубины некротического поражения сердечной мышцы выделяют инфаркт миокарда:
• трансмуральный – с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый).
• интрамуральный – с некрозом в толще миокарда.
• субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду.
• субэпикардиальный – с некрозом миокарда в зоне прилегания к эпикарду.
По изменениям, фиксируемым на ЭКГ, различают.
• «Q-инфаркт» – с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще крупноочаговый трансмуральный инфаркт миокарда).
• «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще мелкоочаговый инфаркт миокарда).
По топографии и в зависимости от поражения определенных ветвей коронарных артерий инфаркт миокарда делится на:
• правожелудочковый.
• левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки.
По кратности возникновения различают инфаркт миокарда:
• первичный.
• рецидивирующий (развивается в срок 8 недель после первичного).
• повторный (развивается спустя 8 недель после предыдущего).
По развитию осложнений инфаркт миокарда подразделяется на:
• осложненный.
• неосложненный По наличию и локализации болевого синдрома.
Выделяют формы инфаркта миокарда:
• типичную – с локализацией боли за грудиной или в прекардиальной области.
• атипичные – с атипичными болевыми проявлениями:
• периферические: леволопаточная, леворучная, гортанно-глоточная, нижнечелюстная, верхнепозвоночная, гастралгическая (абдоминальная).
• безболевые: коллаптоидная, астматическая, отечная, аритмическая, церебральная.
• малосимптомную (стертую).
• комбинированную.
В соответствии с периодом и динамикой развития инфаркта миокарда выделяют:
• стадию ишемии (острейший период).
• стадию некроза (острый период).
• стадию организации (подострый период).
• стадию рубцевания (постинфарктный период).
Симптомы
Около 43% пациентов отмечают внезапное развитие инфаркта миокарда, у большей же части больных наблюдается различный по продолжительности период нестабильной прогрессирующей стенокардии. Острейший период.
Типичные случаи инфаркта миокарда характеризуются чрезвычайно интенсивным болевым синдромом с локализацией болей в грудной клетке и иррадиацией в левое плечо, шею, зубы, ухо, ключицу, нижнюю челюсть, межлопаточную зону. Характер болей может быть сжимающим, распирающим, жгучим, давящим, острым («кинжальным»). Чем больше зона поражения миокарда, тем более выражена боль.
Болевой приступ протекает волнообразно (то усиливаясь, то ослабевая), продолжается от 30 минут до нескольких часов, а иногда и суток, не купируется повторным приемом нитроглицерина. Боль сопряжена с резкой слабостью, возбуждением, чувством страха, одышкой.
Возможно атипичное течение острейшего периода инфаркта миокарда.
У пациентов отмечается резкая бледность кожных покровов, липкий холодный пот, акроцианоз, беспокойство. Артериальное давление в период приступа повышено, затем умеренно или резко снижается по сравнению с исходным (систолическое тахикардия, аритмия.
В этот период может развиться острая левожелудочковая недостаточность (сердечная астма, отек легких). Острый период.
В остром периоде инфаркта миокарда болевой синдром, как правило, исчезает. Сохранение болей бывает вызвано выраженной степенью ишемии околоинфарктной зоны или присоединением перикардита.
В результате процессов некроза, миомаляции и перифокального воспаления развивается лихорадка (от 3-5 до 10 и более дней). Длительность и высота подъема температуры при лихорадке зависят от площади некроза. Артериальная гипотензия и признаки сердечной недостаточности сохраняются и нарастают. Подострый период.
Болевые ощущения отсутствуют, состояние пациента улучшается, нормализуется температура тела. Симптомы острой сердечной недостаточности становятся менее выраженными. Исчезает тахикардия, систолический шум. Постинфарктный период.
В постинфарктном периоде клинические проявления отсутствуют, лабораторные и физикальные данные практически без отклонений. Атипичные формы инфаркта миокарда.
Иногда встречается атипичное течение инфаркта миокарда с локализацией болей в нетипичных местах (в области горла, пальцах левой руки, в зоне левой лопатки или шейно-грудного отдела позвоночника, в эпигастрии, в нижней челюсти) или безболевые формы, ведущими симптомами которых могут быть кашель и тяжелое удушье, коллапс, отеки, аритмии, головокружение и помрачение сознания.
Атипичные формы инфаркта миокарда чаще встречаются у пожилых пациентов с выраженными признаками кардиосклероза, недостаточностью кровообращения, на фоне повторного инфаркта миокарда.
Однако атипично протекает обычно только острейший период, дальнейшее развитие инфаркта миокарда становится типичным.
Возможные осложнения
Нередко осложнения возникают уже в первые часы и дни инфаркта миокарда, утяжеляя его течение. У большинства пациентов в первые трое суток наблюдаются различные виды аритмий: экстрасистолия, синусовая или пароксизмальная тахикардия, мерцательная аритмия, полная внутрижелудочковая блокада. Наиболее опасно мерцание желудочков, которое может перейти в фибрилляцию и привести к гибели пациента.
Левожелудочковая сердечная недостаточность характеризуется застойными хрипами, явлениями сердечной астмы, отека легких и нередко развивается в острейший период инфаркта миокарда. Крайне тяжелой степенью левожелудочковой недостаточности является кардиогенный шок, развивающийся при обширном инфаркте и обычно приводящий к летальному исходу. Признаками кардиогенного шока служит падение систолического АД ниже 80 мм , нарушение сознания, тахикардия, цианоз, уменьшение диуреза.
Разрыв мышечных волокон в зоне некроза может вызывать тампонаду сердца – кровоизлияние в полость перикарда. У 2-3% пациентов инфаркт миокарда осложняется тромбоэмболиями системы легочной артерии (могут стать причиной инфаркта легких или внезапной смерти) или большого круга кровообращения.
Пациенты с обширным трансмуральным инфарктом миокарда в первые 10 суток могут погибнуть от разрыва желудочка вследствие острого прекращения кровообращения. При обширном инфаркте миокарда может возникать несостоятельность рубцовой ткани, ее выбухание с развитием острой аневризмы сердца. Острая аневризма может трансформироваться в хроническую, приводящую к сердечной недостаточности.
Отложение фибрина на стенках эндокарда приводит к развитию пристеночного тромбоэндокардита, опасного возможностью эмболии сосудов легких, мозга, почек оторвавшимися тромботическими массами. В более позднем периоде может развиться постинфарктный синдром, проявляющийся перикардитом, плевритом, артралгиями, эозинофилией.
Диагностика
Среди диагностических критериев инфаркта миокарда важнейшими являются анамнез заболевания, характерные изменения на ЭКГ, показатели активности ферментов сыворотки крови. Жалобы пациента при инфаркте миокарда зависят от формы (типичной или атипичной) заболевания и обширности поражение сердечной мышца. Инфаркт миокарда следует заподозрить при тяжелом и продолжительном (дольше 30-60 минут) приступе загрудинных болей, нарушении проводимости и ритма сердца, острой сердечной недостаточности.
К характерным изменениям ЭКГ относятся формирование отрицательного зубца Т (при мелкоочаговом субэндокардиальном или интрамуральном инфаркте миокарда), патологического комплекса QRS или зубца Q (при крупноочаговом трансмуральном инфаркте миокарда). При ЭхоКГ выявляется нарушение локально сократимости желудочка, истончение его стенки.
В первые 4-6 часов после болевого приступа в крови определяется повышение миоглобина – белка, осуществляющего транспорт кислорода внутрь клеток. Повышение активности креатинфосфокиназы (КФК) в крови более чем на 50% наблюдается спустя 8—10 ч от развития инфаркта миокарда и снижается до нормы через двое суток. Определение уровня КФК проводят через каждые 6-8 часов. Инфаркт миокарда исключается при трех отрицательных результатах.
Для диагностики инфаркта миокарда на более поздних сроках прибегают к определению фермента лактатдегидрогеназы (ЛДГ), активность которой повышается позже КФК – спустя 1-2 суток после формирования некроза и приходит к нормальным значениям через 7-14 дней. Высокоспецифичным для инфаркта миокарда является повышение изоформ миокардиального сократительного белка тропонина – тропонина-Т и тропонина-1, увеличивающихся также при нестабильной стенокардии. В крови определяется увеличение СОЭ, лейкоцитов, активности аспартатаминотрансферазы (АсАт) и аланинаминотрансферазы (АлАт).
Коронарная ангиография (коронарография) позволяет установить тромботическую окклюзию коронарной артерии и снижение желудочковой сократимости, а также оценить возможности проведения аортокоронарного шунтирования или ангиопластики – операций, способствующих восстановлению кровотока в сердце.
Лечение
При инфаркте миокарда показана экстренная госпитализация в кардиологическую реанимацию. В остром периоде пациенту предписывается постельный режим и психический покой, дробное, ограниченное по объему и калорийности питание. В подостром периоде больной переводится из реанимации в отделение кардиологии, где продолжается лечение инфаркта миокарда и осуществляется постепенное расширение режима.
Купирование болевого синдрома проводится сочетанием наркотических анальгетиков (фентанила) с нейролептиками (дроперидолом), внутривенным введением нитроглицерина.
Терапия при инфаркте миокарда направлена на предупреждение и устранение аритмий, сердечной недостаточности, кардиогенного шока. Назначают антиаритмические средства (лидокаин), ß-адреноблокаторы (атенолол), тромболитики (гепарин, ацетилсалициловая к-та), антогонисты Са (верапамил), магнезию, нитраты, спазмолитики.
В первые 24 часа после развития инфаркта миокарда можно произвести восстановление перфузии путем тромболизиса или экстренной баллонной коронарной ангиопластики.
Прогноз
Инфаркт миокарда является тяжелым, сопряженным с опасными осложнениями заболеванием. Большая часть летальных исходов развивается в первые сутки после инфаркта миокарда. Насосная способность сердца связана с локализацией и объемом зоны инфаркта. При повреждении более 50% миокарда, как правило, сердце функционировать не может, что вызывает кардиогенный шок и гибель пациента. Даже при менее обширном повреждении сердце не всегда справляется нагрузками, в результате чего развивается сердечная недостаточность.
По истечении острого периода прогноз на выздоровление хороший. Неблагоприятные перспективы у пациентов с осложненным течением инфаркта миокарда.
Профилактика
Необходимыми условиями профилактики инфаркта миокарда являются ведение здорового и активного образа жизни, отказ от алкоголя и курения, сбалансированное питание, исключение физического и нервного перенапряжения, контроль АД и уровня холестерина крови.
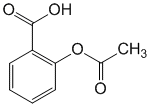
Названия
Русское название: Ацетилсалициловая кислота.
Английское название: Acetylsalicylic acid.
Латинское название
Acidum acetylsalicylicum ( Acidi acetylsalicylici).
Химическое название
2-(Ацетилокси)бензойная кислота.
Фарм Группа
• Антиагреганты.
• НПВС — Производные салициловой кислоты.
 Нозологии
Нозологии
• G43 Мигрень.
• G54,3 Поражения грудных корешков, не классифицированные в других рубриках.
• I20,0 Нестабильная стенокардия.
• I21,9 Острый инфаркт миокарда неуточненный.
• I24,1 Синдром Дресслера.
• I25 Хроническая ишемическая болезнь сердца.
• I25,5 Ишемическая кардиомиопатия.
• I25,8 Другие формы хронической ишемической болезни сердца.
• I26,9 Легочная эмболия без упоминания об остром легочном сердце.
• I34,0 Митральная (клапанная) недостаточность.
• I34,1 Пролапс [пролабирование] митрального клапана.
• I49,8 Другие уточненные нарушения сердечного ритма.
• I63 Инфаркт мозга.
• I74,9 Эмболия и тромбоз неуточненных артерий.
• I77,6 Артериит неуточненный.
• I80 Флебит и тромбофлебит.
• K08,8,0* Боль зубная.
• M25,5 Боль в суставе.
• M54,4 Люмбаго с ишиасом.
• M79,1 Миалгия.
• M79,2 Невралгия и неврит неуточненные.
• N94,6 Дисменорея неуточненная.
• R50 Лихорадка неясного происхождения.
• R51 Головная боль.
• Z100* КЛАСС XXII Хирургическая практика.
Код CAS
50-78-2.
Характеристика вещества
Белые мелкие игольчатые кристаллы или легкий кристаллический порошок без запаха или со слабым запахом, слабокислого вкуса. Мало растворим в воде при комнатной температуре, растворим в горячей воде, легко растворим в этаноле, растворах едких и углекислых щелочей.
Фармакодинамика
Фармакологическое действие – противовоспалительное, жаропонижающее, антиагрегационное, анальгезирующее.
Ингибирует циклооксигеназу (ЦОГ-1 и ЦОГ-2) и необратимо тормозит циклооксигеназный путь метаболизма арахидоновой кислоты, блокирует синтез ПГ (ПГA2, ПГD2, ПГF2aльфа, ПГE1, ПГE2 и тд;) и тромбоксана. Уменьшает гиперемию, экссудацию, проницаемость капилляров, активность гиалуронидазы, ограничивает энергетическое обеспечение воспалительного процесса путем угнетения продукции АТФ. Влияет на подкорковые центры терморегуляции и болевой чувствительности. Снижение содержания ПГ (преимущественно ПГЕ1 ) в центре терморегуляции приводит к понижению температуры тела вследствие расширения сосудов кожи и увеличения потоотделения. Обезболивающий эффект обусловлен влиянием на центры болевой чувствительности, а также периферическим противовоспалительным действием и способностью салицилатов снижать альгогенное действие брадикинина. Уменьшение содержания тромбоксана А2 в тромбоцитах приводит к необратимому подавлению агрегации, несколько расширяет сосуды. Антиагрегантное действие сохраняется в течение 7 суток после однократного приема. В ходе ряда клинических исследований показано, что существенное ингибирование склеиваемости кровяных пластинок достигается при дозах до 30 мг. Увеличивает фибринолитическую активность плазмы и снижает концентрацию витамин K-зависимых факторов свертывания (II, VII, IX, X). Стимулирует выведение мочевой кислоты, поскольку нарушается ее реабсорбция в канальцах почек.
После приема внутрь достаточно полно всасывается. При наличии кишечнорастворимой оболочки (устойчива к действию желудочного сока и не допускает всасывания ацетилсалициловой кислоты в желудке) абсорбируется в верхнем отделе тонкого кишечника. Во время абсорбции подвергается пресистемной элиминации в стенке кишечника и в печени (деацетилируется). Абсорбированная часть очень быстро гидролизуется специальными эстеразами, поэтому T1/2 ацетилсалициловой кислоты составляет не более 15–20 мин. В организме циркулирует (на 75–90% в связи с альбумином) и распределяется в тканях в виде аниона салициловой кислоты. Cmax достигается примерно через 2 C белками плазмы крови ацетилсалициловая кислота практически не связывается. При биотрансформации в печени образуются метаболиты, обнаруживаемые во многих тканях и моче. Экскреция салицилатов осуществляется преимущественно путем активной секреции в канальцах почек в неизмененной форме и в виде метаболитов. Выведение неизмененного вещества и метаболитов зависят от pH мочи (при подщелачивании мочи возрастает ионизирование салицилатов, ухудшается их реабсорбция и значительно увеличивается экскреция).
Показания к применению
ИБС. Наличие нескольких факторов риска ИБС. Безболевая ишемия миокарда. Нестабильная стенокардия. Инфаркт миокарда (для снижения риска повторного инфаркта миокарда и смерти после инфаркта миокарда). Повторная преходящая ишемия мозга и ишемический инсульт у мужчин. Протезирование клапанов сердца (профилактика и лечение тромбоэмболий). Баллонная коронарная ангиопластика и установка стента (снижение риска повторного стеноза и лечение вторичного расслоения коронарной артерии). А также при неатеросклеротических поражениях коронарных артерий (болезнь Кавасаки). Аортоартериит (болезнь Такаясу). Клапанные митральные пороки сердца и мерцательная аритмия. Пролапс митрального клапана (профилактика тромбоэмболии). Рецидивирующие тромбоэмболии легочной артерии. Синдром Дресслера. Инфаркт легкого. Острый тромбофлебит. Лихорадка при инфекционно-воспалительных заболеваниях. Болевой синдром слабой и средней интенсивности различного генеза, в тч грудной корешковый синдром, люмбаго, мигрень, головная боль, невралгия, зубная боль, миалгия, артралгия, альгодисменорея. В клинической иммунологии и аллергологии используется в постепенно нарастающих дозах для продолжительной «аспириновой» десенситизации и формирования стойкой толерантности к НПВС у больных с «аспириновой» астмой и «аспириновой» триадой.
По показаниям ревматизм, ревматическая хорея, ревматоидный артрит, инфекционно-аллергический миокардит, перикардит — в настоящее время применяется очень редко.
Противопоказания
Гиперчувствительность. В тч «аспириновая» триада. «аспириновая» астма; геморрагический диатез (гемофилия. Болезнь Виллебранда. Телеангиоэктазия). Расслаивающая аневризма аорты. Сердечная недостаточность. Острые и рецидивирующие эрозивно-язвенные заболевания ЖКТ. Желудочно-кишечное кровотечение. Острая почечная или печеночная недостаточность. Исходная гипопротромбинемия. Дефицит витамина К. Тромбоцитопения. Тромботическая тромбоцитопеническая пурпура. Дефицит глюкозо-6-фосфатдегидрогеназы. Беременность (I и III триместр). Грудное вскармливание. Детский и подростковый возраст до 15 лет при применении в качестве жаропонижающего средства (риск развития синдрома Рейе у детей с лихорадкой на фоне вирусных заболеваний).
Ограничения к использованию
Гиперурикемия, нефролитиаз, подагра, язвенная болезнь желудка и двенадцатиперстной кишки (в анамнезе), тяжелые нарушения функции печени и почек, бронхиальная астма, ХОБЛ, полипоз носа, неконтролируемая артериальная гипертензия.
Применение при беременности и кормлении грудью
Применение больших доз салицилатов в I триместре беременности ассоциируется с повышенной частотой дефектов развития плода (расщепление неба, пороки сердца). Во II триместре беременности салицилаты можно назначать только с учетом оценки риска и пользы. Назначение салицилатов в III триместре беременности противопоказано.
Салицилаты и их метаболиты в небольших количествах проникают в грудное молоко. Случайный прием салицилатов в период лактации не сопровождается развитием побочных реакций у ребенка и не требует прекращения грудного вскармливания. Однако при длительном применении или назначении в высоких дозах кормление грудью следует прекратить.
Побочные эффекты
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): тромбоцитопения, анемия, лейкопения.
Со стороны органов ЖКТ. НПВС – гастропатия (диспепсия, боль в эпигастральной области, изжога, тошнота и рвота, тяжелые кровотечения в ЖКТ), снижение аппетита.
Аллергические реакции. Реакции гиперчувствительности (бронхоспазм. Отек гортани и крапивница). Формирование на основе гаптенового механизма «аспириновой» бронхиальной астмы и «аспириновой» триады (эозинофильный ринит. Рецидивирующий полипоз носа. Гиперпластический синусит).
Прочие. Нарушение функции печени и/или почек, синдром Рейе у детей (энцефалопатия и острая жировая дистрофия печени с быстрым развитием печеночной недостаточности).
При длительном применении — головокружение. Головная боль. Шум в ушах. Снижение остроты слуха. Нарушение зрения. Интерстициальный нефрит. Преренальная азотемия с повышением уровня креатинина крови и гиперкальциемией. Папиллярный некроз. Острая почечная недостаточность. Нефротический синдром. Заболевания крови. Асептический менингит. Усиление симптомов застойной сердечной недостаточности. Отеки. Повышение уровня аминотрансфераз в крови.
Взаимодействие
Усиливает токсичность метотрексата, снижая его почечный клиренс, эффекты наркотических анальгетиков (кодеин), пероральных противодиабетических препаратов, гепарина, непрямых антикоагулянтов, тромболитиков и ингибиторов агрегации тромбоцитов, снижает эффект урикозурических ЛС (бензбромарон, сульфинпиразон), гипотензивных средств, диуретиков (спиронолактон, фуросемид). Парацетамол, кофеин повышают риск развития побочных явлений. Глюкокортикоиды, этанол и этанолсодержащие ЛС усиливают негативное воздействие на слизистую оболочку ЖКТ и увеличивают клиренс. Повышает концентрацию дигоксина, барбитуратов, солей лития в плазме. Антациды, содержащие магний и/или алюминий, замедляют и ухудшают всасывание ацетилсалициловой кислоты. Миелотоксические ЛС усиливают проявления гематотоксичности ацетилсалициловой кислоты.
Передозировка
Может возникать после однократного приема большой дозы или при длительном употреблении. Если однократная доза меньше 150 мг/кг, острое отравление считают легким, 150–300 мг/кг — умеренным, при употреблении более высоких доз — тяжелым.
Симптомы. Синдром салицилизма (тошнота, рвота, шум в ушах, нарушение зрения, головокружение, сильная головная боль, общее недомогание, лихорадка – плохой прогностический признак у взрослых). Более тяжелое отравление — ступор, судороги и кома, некардиогенный отек легких, резкая дегидратация, нарушения КЩС (вначале — респираторный алкалоз, затем — метаболический ацидоз), почечная недостаточность и шок.
При хронической передозировке концентрация, определяемая в плазме, плохо коррелирует со степенью тяжести интоксикации. Наибольший риск развития хронической интоксикации отмечается у людей пожилого возраста при приеме в течение нескольких суток более 100 мг/кг/сут. У детей и пациентов пожилого возраста начальные признаки салицилизма не всегда заметны, поэтому целесообразно периодически определять концентрацию салицилатов в крови. Уровень выше 70 мг% свидетельствует об умеренном или тяжелом отравлении; выше 100 мг% — о крайне тяжелом, прогностически неблагоприятном. При отравлении средней тяжести необходима госпитализация по крайней мере на 24.
Лечение. Провокация рвоты, назначение активированного угля и слабительных, мониторирование КЩС и электролитного баланса; в зависимости от состояния обмена веществ – введение натрия гидрокарбоната, раствора натрия цитрата или натрия лактата. Повышение резервной щелочности усиливает выведение ацетилсалициловой кислоты за счет ощелачивания мочи. Ощелачивание мочи показано при уровне салицилатов выше 40 мг%, обеспечивается в/в инфузией гидрокарбоната натрия — 88 мэкв в 1 л 5% раствора глюкозы, со скоростью 10–15 мл/кг/ Восстановление ОЦК и индукция диуреза (достигается введением гидрокарбоната в той же дозе и разведении, повторяют 2–3 раза); следует иметь в виду, что интенсивная инфузия жидкости пожилым больным может привести к отеку легких. Не рекомендуется применение ацетазоламида для ощелачивания мочи (может вызывать ацидемию и усиливать токсическое действие салицилатов). Гемодиализ показан при уровне салицилатов более 100–130 мг%, а у больных с хроническим отравлением — 40 мг% и ниже при наличии показаний (рефрактерный ацидоз, прогрессирующее ухудшение состояния, тяжелое поражение ЦНС, отек легких и почечная недостаточность). При отеке легких — ИВЛ смесью, обогащенной кислородом, в режиме положительного давления в конце выдоха; для лечения отека мозга применяют гипервентиляцию и осмотический диурез.
Способ применения и дозы
Внутрь.
Меры предосторожности применения
Нежелательно совместное применение с другими НПВС и глюкокортикоидами. За 5–7 суток до хирургического вмешательства необходимо отменить прием (для уменьшения кровоточивости в ходе операции и в послеоперационном периоде).
Вероятность развития НПВС-гастропатии снижается при назначении после еды, использовании таблеток с буферными добавками или покрытых специальной кишечнорастворимой оболочкой. Риск геморрагических осложнений считается наименьшим при применении в дозах.
Следует учитывать, что у предрасположенных пациентов ацетилсалициловая кислота (даже в небольших дозах) уменьшает выведение мочевой кислоты из организма и может стать причиной развития острого приступа подагры.
Во время длительной терапии рекомендуется регулярно производить анализ крови и исследовать кал на скрытую кровь. В связи с наблюдавшимися случаями гепатогенной энцефалопатии не рекомендуется для купирования лихорадочного синдрома у детей.
Первая помощь при инфаркте
Последовательность действий изложена в виде алгоритма:
- Немедленно вызвать скорую помощь – медицинский персонал обладает необходимыми для поддержания жизнедеятельности пациента навыками, средствами экстренной помощи и возможностью быстрой диагностики (могут провести ЭКГ и подтвердить инфаркт, уточнить его степень поражения и локализацию для дальнейших действий в клинике).
- Необходимо посадить пациента, или перевести его в полулежачее положение. В помещении следует открыть окно, с больного снять лишнюю одежду – он нуждается в большом количестве кислорода.
- Можно дать больному таблетку Нитроглицерина или Аспирина– первый препарат расширит коронарные сосуды, а второй не дает крови быстро свернуться, образовав тромб. Допустим прием успокоительных средств.
- До прибытия скорой находиться возле пациента и стараться его успокоить.
Описание

Инфаркт миокарда. Очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом.
Дополнительные факты
Инфаркт миокарда. Очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом.
Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход. В возрасте 40-60 лет инфаркт миокарда в 3–5 раз чаще наблюдается у мужчин в связи с более ранним (на 10 лет раньше, чем у женщин) развитием атеросклероза.
После 55-60 лет заболеваемость среди лиц обоего пола приблизительно одинакова. Показатель летальности при инфаркте миокарда составляет 30—35%. Статистически 15—20% внезапных смертей обусловлены инфарктом миокарда. Нарушение кровоснабжения миокарда на 15-20 и более минут приводит к развитию необратимых изменений в сердечной мышце и расстройству сердечной деятельности.
Острая ишемия вызывает гибель части функциональных мышечных клеток (некроз) и последующее их замещение волокнами соединительной ткани, т. Е. Формирование постинфарктного рубца. В клиническом течении инфаркта миокарда выделяют пять периодов: • 1 период. Предынфарктный (продромальный) – учащение и усиление приступов стенокардии, может продолжаться несколько часов, суток, недель; • 2 период.
Острейший – от развития ишемии до появления некроза миокарда, продолжается от 20 минут до 2 часов; • 3 период. Острый – от образования некроза до миомаляции (ферментативного расплавления некротизированной мышечной ткани), длительность от 2 до 14 суток; • 4 период. Подострый – начальные процессы организации рубца, развитие грануляционной ткани на месте некротической, продолжительность 4 – 8 недель; • 5 период. Постинфарктный – созревание рубца, адаптация миокарда к новым условиям функционирования.
Диагностика
Диагностика начинается с общего осмотра, аускультации сердечных шумов и сбора анамнеза. Уже в карете скорой помощи можно провести ЭКГ и поставить предварительный диагноз. Там же начинается и первое симптоматическое лечение – наркотические анальгетики вводятся для профилактики кардиогенного шока.

В условиях стационара проводят эхокардиограмму сердца, которая позволит увидеть полную картину инфаркта, его локализацию, глубину повреждений, характер нарушений в работе сердца по отношению к потокам крови внутри него.
Лабораторные исследования предполагают назначение биохимического анализа крови на специфические маркеры некроза миокарда – КФК-МВ, ЛДГ1,5, С-реактивный белок.
Среди диагностических критериев инфаркта миокарда важнейшими являются анамнез заболевания, характерные изменения на ЭКГ, показатели активности ферментов сыворотки крови. Жалобы пациента при инфаркте миокарда зависят от формы (типичной или атипичной) заболевания и обширности поражение сердечной мышца.
Инфаркт миокарда следует заподозрить при тяжелом и продолжительном (дольше 30-60 минут) приступе загрудинных болей, нарушении проводимости и ритма сердца, острой сердечной недостаточности. К характерным изменениям ЭКГ относятся формирование отрицательного зубца Т (при мелкоочаговом субэндокардиальном или интрамуральном инфаркте миокарда), патологического комплекса QRS или зубца Q (при крупноочаговом трансмуральном инфаркте миокарда).
При ЭхоКГ выявляется нарушение локально сократимости желудочка, истончение его стенки. В первые 4-6 часов после болевого приступа в крови определяется повышение миоглобина – белка, осуществляющего транспорт кислорода внутрь клеток. Повышение активности креатинфосфокиназы (КФК) в крови более чем на 50% наблюдается спустя 8—10 ч от развития инфаркта миокарда и снижается до нормы через двое суток.
Определение уровня КФК проводят через каждые 6-8 часов. Инфаркт миокарда исключается при трех отрицательных результатах. Для диагностики инфаркта миокарда на более поздних сроках прибегают к определению фермента лактатдегидрогеназы (ЛДГ), активность которой повышается позже КФК – спустя 1-2 суток после формирования некроза и приходит к нормальным значениям через 7-14 дней.
Высокоспецифичным для инфаркта миокарда является повышение изоформ миокардиального сократительного белка тропонина – тропонина-Т и тропонина-1, увеличивающихся также при нестабильной стенокардии. В крови определяется увеличение СОЭ, лейкоцитов, активности аспартатаминотрансферазы (АсАт) и аланинаминотрансферазы (АлАт).
Прогноз
Инфаркт миокарда является тяжелым, сопряженным с опасными осложнениями заболеванием. Большая часть летальных исходов развивается в первые сутки после инфаркта миокарда. Насосная способность сердца связана с локализацией и объемом зоны инфаркта. При повреждении более 50% миокарда, как правило, сердце функционировать не может, что вызывает кардиогенный шок и гибель пациента.

